脂质体转染
脂质体(lipofectin regeant,LR)试剂是阳离子脂质体N-[1-2,3-Dioleyoxy,Propyl]-n, n,n-Trimethylammonium Chloride(DOTMA)和Dioleoyl photidye-thanolamine(DOPE)的混合物[1:1(w/w)]。它适用于把DNA转染入悬浮或贴壁培养细胞中,是目前条件下最方便的转染方法之一。转染率高,优于磷酸钙法,比它高5~100倍,能把DNA和RNA转染到各种细胞。COS-7、BHK、NIH3T3、Hela和Jurkat等任何一种细胞均可作为受体细胞。
脂质体转染原理
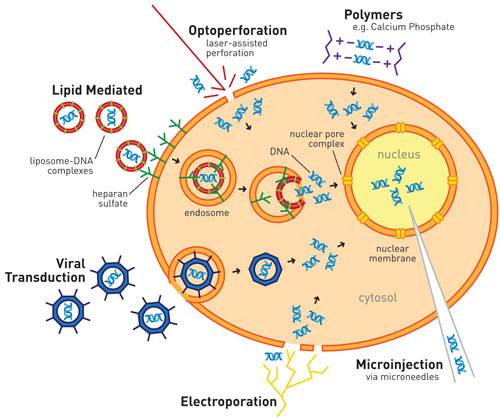
脂质体转染方法原理:阳离子脂质体表面带正电荷,能与核酸的磷酸根通过静电作用将DNA分子包裹人内,形成DNA-脂复合体,也能被表面带负电荷的细胞膜吸附,再通过膜的融合或细胞的内吞作用,偶尔也通过直接渗透作用,DNA传递进入细胞,形成包涵体或进入溶酶体 其中一小部分DNA能从包涵体内释放,并进入细胞质中,再进一步进入核内转录、表达。
脂质体转染操作步骤
操作步骤[方法一]:
细胞培养:取6孔培养板(或用35mm培养皿),向每孔中加入2mL含1~2×105个细胞培养液,37℃CO2培养至40%~60%汇合时(汇合过分,转染后不利筛选细胞)。
转染液制备:在聚苯乙稀管中制备以下两液(为转染每一个孔细胞所用的量)A液:用不含血清培养基稀释1-10μg DNA,终量100μL,B液:用不含血清培养基稀释2-50μgLR,终量100μL,轻轻混合A、B液,室温中置10-15分钟,稍后会出现微浊现象,但并不妨碍转染(如出现沉淀可能因LR或DNA浓度过高所致,应酌情减量)。
转染准备:用2mL不含血清培养液漂洗两次,再加入1mL不含血清培养液。
转染:把A/B复合物缓缓加入培养液中,摇匀,37℃温箱置6~24小时,吸除无血清转染液,换入正常培养液继续培养。
其余处理如观察、筛选、检测等与其它转染法相同。
注意:转染时切勿加血清,血清对转染效率有很大影响。
快速脂质体转染法 [方法二]:
以5×105细胞/孔接种6孔板(或35mm培养皿)培养24小时,使其达到50~60%板底面积。
在试管中配制DNA/脂质体复合物方法如下:
在1mL无血清DMEM中稀释PSV2-neo质粒DNA或供体DNA。旋转1秒钟,再加入脂质体悬液,旋转。室温下放置5~10分钟,使DNA结合在脂质体上。
弃去细胞中的旧液,用1mL无血清DMEM洗细胞一次后弃去,向每孔中直接加入1mL DNA/脂质体复合物,37℃培养3~5小时。
再于每孔中加入20%FCS的DMEM,继续培养14~24小时。
吸出DMEM/DNA/脂质体混合物加入新鲜10%FCS的DMEM,2mL/孔,再培养24~48小时。
用细胞刮或消化法收集细胞,以备分析鉴定。
稳定的脂质体转染方法:
接种细胞同前,细胞长至50%板底面积可用于转染。
DNA/脂质体复合物制备转染细胞同前(2)、(3)步骤。
在每孔中加入1mL、20%FCS的DMEM,37℃培养48小时。
吸出DMEM,用G418选择培养液稀释细胞,使细胞生长一定时间,筛选转染克隆,方法参照细胞克隆筛选法进行。
Lipofectamine2000在24孔板转染单层贴壁细胞方法如下:
转染前1天将0.5~2×105细胞接种于24孔培养板,并加入500ul不含抗生素的完全培养基,以保证转染时细胞汇合达90~95%。
准备复合物
将0.8ug DNA稀释于50ul无血清无抗生素的培养液中轻轻浑匀。
将2ul Lipofectamine2000稀释于50ul无血清无抗生素的培养液中,轻轻浑匀,室温孵育5分。
5分后将它们混合,并轻轻浑匀,室温孵育20分。
吸去培养板的培养基,用PBS或无血清培养基(最好)清洗细胞2次。
将复合物(总体积100ul)加入培养孔,前后摇动培养板使其分布均匀。
将细胞放入培养箱孵育4~6h后,可以更换含血清培养液去除复合物(也可不用)。
24~48h后可以观察转入基因表达情况。
稳定转染:换含血清培养基24h后将细胞以1:10(或更高比例)传代,1天后更换筛选培养基筛选。
优化:要保证细胞汇合率达90~95%(比较高);DNA/ Lipofectamine2000比率1:0.5~1:5,一般细胞1:2~3。